Резюме. У статті подано огляд даних світової літератури стосовно уражень нервової системи в пацієнтів, які перенесли COVID-19. Також наведені результати власного відкритого порівняльного дослідження ефективності комплексного застосування Ксаврону, Тіворелю й Ксилату в пацієнтів з неврологічними порушеннями в постковідному періоді. Був продемонстрований позитивний вплив вищезазначеного комплексу препаратів на когнітивні функції, що виражалось в збільшенні темпу психічної діяльності, покращанні короткочасної і оперативної пам’яті, підвищенні стійкості психічних процесів і зниженні рівнів реактивної та особистісної тривожності.
Пандемія, викликана COVID-19, — тема, що зараз перебуває в центрі уваги світової медичної спільноти [1–4]. Крім респіраторного синдрому, вірус COVID-19 викликає пошкодження серцево-судинної системи, нирок, суглобів, нервової системи [5–16].
Перші дані щодо неврологічних порушень на фоні COVID-19 з’явились уже в березні 2020 року. Китайські лікарі Н. Mао, Н. Jin, М. Wang et al. у журналі JAMA Neurol опублікували дані власних досліджень, які свідчили про те, що в 45,5 % пацієнтів з COVID-19 спостерігаються неврологічні порушення у вигляді головокружіння (у 19,3 % хворих), головного болю (у 17,1 %), порушення свідомості (у 14,8 %), гіпогевзії (у 5,5 %), гіпосмії (у 5,1 %), скелетно-м’язових розладів (у 19,3 %), мозкових інсультів (у 6,8 %) [17].
У подальшому клінічні спостереження, проведені в інших країнах світу, показали, що частота зустрічальності неврологічних порушень становить від 40 до 60 % у хворих на COVID-19 [18–36]. Так, мультицентрове дослідження, яке було проведено на півночі Португалії з березня по червень 2020 року, показало, що серед 1261 госпіталізованого пацієнта з COVID-19 36,2 % мали неврологічні порушення. У 13,4 % був головний біль, у 10,1 % — тривожні розлади, у 9,7 % — порушення свідомості. Гострі ушкодження центральної нервової системи спостерігались у 19,1 % хворих, що становило 217 випадків на 1000 госпіталізованих у цьому регіоні [37].
Клінічна практика показала, що неврологічні розлади є частими у хворих на COVID-19 і підвищують ступінь інвалідизації. Про пошкодження нервової системи повідомляють лікарі з усіх країн світу. При цьому неврологічні розлади розвиваються з боку як центральної, так і периферичної і м’язової систем [6, 7, 10, 38].
Порушення центральної нервової системи у хворих на COVID-19 проявляються у вигляді головокружіння, головного болю, порушень свідомості, запальних захворювань (менінгоенцефаліти, менінгіти, енцефаліти, мієліти), демієлінізуючих захворювань (розсіяний склероз, дисемінований енцефаломієліт), гострої некротичної енцефалопатії, нейродегенеративних захворювань (хвороба Паркінсона, хвороба Альцгеймера), гіпоксичної енцефалопатії, цереброваскулярних захворювань (ішемічний інсульт, внутрішньомозковий крововилив, субарахноїдальний крововилив, венозний тромбоз, транзиторні ішемічні атаки, хронічна ішемія мозку) [14, 39–45].
Ураження периферичної нервової системи хворих на COVID-19 проявляється гіпогевзією, гіпосмією, мононейропатією, краніальною полінейропатією, синдромом Гієна — Барре, синдромом Міллера — Фішера, невралгіями [31, 46, 47].
Часто у хворих на COVID-19 спостерігаються ураження м’язової системи, а саме міалгії, міопатії, скелетно-м’язові болі [48, 49].
Яким же чином вірус потрапляє до нервової системи? Досі точиться дискусія відносно шляхів потрапляння вірусу до центральної нервової системи. На сьогодні є докази, що вірус SARS-CoV-2 проникає в нервові клітини через рецептори ACE2. Можливі й інші шляхи — за рахунок прямої інвазії вірусу в нервову тканину, гіпоксії, сепсису, мультиорганного ураження, цитокінового шторму тощо.
Можна виділити 2 основні шляхи потрапляння вірусу до центральної нервової системи — гематогенний і нейрогенний [50–54]. Потрапивши в центральну нервову систему, вірус може інфікувати астроцити, мікроглію, активувати каскад нейрозапалення й нейродегенерацію за рахунок вивільнення цитокінів, фактора некрозу пухлини (TNF) та інших медіаторів запалення [51]. У багатьох випадках відбувається дисемінація SARS-CoV-2 через нюхові цибулини, а від них — до гіпоталамуса. Попадання вірусу до нервової системи призводить до розвитку неврологічних захворювань або загострення уже існуючих хвороб [40, 54].
Гостра необхідність у більш глибокому розумінні неврологічних проблем, пов’язаних з COVID-19, привела до створення за ініціативи Європейської академії неврології (EAN) нейробанку даних COVID-19 (NeuroCOVID) — бази даних, що збирає клінічну інформацію про неврологічні симптоми, ускладнення й наслідки, пов’язані із зараженням SARS-CoV-2, а також про вплив COVID-19 на перебіг уже існуючих неврологічних захворювань.
Динамічні спостереження за хворими показали, що і після гострого періоду захворювання спостерігаються порушення з боку серцево-судинної, нервової систем, нирок тощо, які ще довго зберігаються в частини хворих, або з’являються нові симптоми протягом декількох місяців. Так, було проаналізовано перебіг захворювання у 47 780 хворих на COVID-19 після виписки із стаціонарів.
У третини пацієнтів через 140 днів спостерігались порушення з боку нирок, серцево-судинної системи, респіраторні розлади, цукровий діабет, неврологічні розлади. Такі порушення частіше виникають у людей похилого віку [55]. Лікарі стали описувати цей стан як постковідний синдром, тривалий COVID-19, підгострий COVID-19, віддалені ефекти COVID-19 [56].
У грудні 2020 року Національним інститутом здоров’я Великої Британії (NICE) була запропонована класифікація ковідних станів: гострий COVID-19 (симптоми, що тривають до 4 тижнів); тривалий симптоматичний COVID-19 (симптоми, що тривають від 4 до 12 тижнів); постковідний синдром (симптоми, що тривають понад 12 тижнів, вони здатні змінюватися з часом, зникати й знову виникати, зачіпаючи багато систем організму) [57].
Постковідний синдром внесений до Міжнародного класифікатора хвороб (МКХ-10) у формулюванні Post COVID-19 condition.
У цей же час було запропоновано термін PostCOVID long hauler. Ідеться про будь-яку людину, у якої діагностовано коронавірус, що викликав COVID-19, яка не повернулась до свого рівня здоров’я і функціонування через 12 тижнів після перенесеного захворювання. При цьому наявність постковідного синдрому не завжди залежить від ступеня тяжкості перебігу гострого періоду COVID-19.
Частими проявами постковідного синдрому є неврологічні, психічні порушення, що суттєво впливають на якість життя пацієнтів. У метааналізі S. Loper-Leon et al., що включав 15 досліджень із залученням 47 970 пацієнтів, які перенесли COVID-19, показано, що астенія зустрічалась у 58 % хворих, зниження концентрації уваги — у 27 %, порушення пам’яті — у 16 % [58].
Італійські лікарі провели аналіз 402 пацієнтів (середній вік 58 років) через 1 місяць після стаціонарного лікування. У 56 % хворих був хоча б 1 неврологічний симптом. Часто у хворих виявлялись психічні порушення. Так, депресія була в 31 % хворих, порушення сну — у 40 %, тривога — у 42 %, посттравматичні розлади — у 28 % [59].
Дослідження, проведені через два місяці після лікування, показали, що тільки 13–15 % пацієнтів були повністю безсимптомними. Близько 30 % пацієнтів мали 1 або 2 залишкових симптоми. У 50 % хворих було 3 або більше симптоми. У цілому у 2/3 пацієнтів спостерігались неврологічні порушення [60, 61].
Найбільш частими симптомами після COVID-19 були втомлюваність, порушення пам’яті, уваги, нічного сну, емоційна нестабільність, задишка. До типових симптомів постковідного синдрому також належать біль у м’язах і суглобах, стійка втрата смаку й нюху [62].
Інші автори повідомили, що найбільш частими неврологічними розладами в постковідному періоді є: аносмія/агевзія (у 59 % на початку захворювання, у 28 % — на 30-й і у 23 % — на 60-й день); задишка (у 36,7 % — на 30-й день і в 30 % — на 60-й день); астенія (у 50 % — на 30-й день і в 40 % — на 60-й день). Наявність стійких симптомів на 60-й день частіше спостерігалася в осіб віком від 40 до 60 років, а тяжкий перебіг COVID-19 і задишка на початку захворювання були асоційовані з наявністю стійких симптомів на 30-й день [63].
Аналіз проведених досліджень показав, що залишкова симптоматика значною мірою залежить від віку пацієнта, тривалості перебування в лікарні, тяжкості перебігу й наявності задишки на початку захворювання [63].
Проведення позитронно-емісійної томографії в пацієнтів, які перенесли коронавірус, у яких функціональні скарги зберігалися через 3 тижні після появи перших симптомів інфекції, продемонстрували зниження метаболізму головного мозку в ділянці нюхової звивини, у зонах лімбічної і паралімбічної ділянок, у стовбурі мозку й мозочка [62–64].
Отже, як свідчить клінічна практика, порушення нервової системи, які розвинулись під час COVID-19, не минають безслідно, можуть тривати невизначено довгий час, що обумовлено структурними змінами головного мозку, які виникають внаслідок вірусу SARS-CoV-2.
Продовжують вивчатись причини розвитку неврологічних порушень у постковідному періоді. Експериментальні й клінічні дослідження свідчать про те, що у хворих у постковідному періоді спостерігаються явища «тліючого» системного запалення (наслідки системної гіперімунної відповіді), ендотеліїту (генералізоване запальне ураження судин), пульмоніту (пошкодження легень унаслідок ураження судин та альвеолоцитів вірусом і цитокінами), контрінсулярного ефекту дексаметазону (енергодефіцит та астенізація) та ін. [62–64].
У постковідному періоді розвиток системного «тліючого» запалення виникає внаслідок ушкодження цитокінами й вільними радикалами ендотелію судин при гіперімунній реакції (Varga et al., 2020); у пацієнтів після одужання концентрація цитокінів у сироватці крові (інтерлейкін (IL) -2, -4, -6, -17) була вищою порівняно з контрольною групою, що свідчить про продовження запального процесу після одужання (Hasichaolu et al., 2020).
Цитокіни здатні збільшувати проникність гематоенцефалічного бар’єра, забезпечуючи проникнення вірусу в мозок [65].
Є непрямі механізми залучення мозку, які включають:
- порушення регуляції цитокінів — доведено, що прозапальні цитокіни, зокрема інтерлейкін-6 і фактор некрозу пухлини, пов’язані з розвитком енцефаліту на тлі цитокінового шторму;
- міграцію імунних клітин з периферії за механізмом «троянського коня», що спричинює запалення в нервових клітинах і вірус-індуковану невропатію;
- автоімунну агресію;
- гіпоксичну травму через безпосередній вплив коронавірусу на дихальний і серцево-судинний центри довгастого мозку. Гіпоксія головного мозку спричинює активацію анаеробного метаболізму, через що й виникає набряк мозку, знижується мозковий кровоток, підвищується внутрішньочерепний тиск, розвиваються неврологічні й психіатричні симптоми;
- тромботичну мікроангіопатію, що спричинює продукування антитіл проти кардіоліпіну, ушкодження мозку за участю антифосфоліпідних антитіл [65].
Також коронавірус може спричинити тяжкі ураження мозку (інсульти, енцефаліти тощо) у пацієнтів, які страждають від неврологічних розладів, включно з параноєю і галюцинаціями [66]. Спостерігаються й численні поведінкові відхилення, що свідчать про ураження головного мозку [67], за аналогією з іншими коронавірусними хворобами (тяжкий гострий респіраторний синдром і близькосхідний коронавірусний респіраторний синдром) науковці прогнозують довгострокові наслідки запалення головного мозку в деяких хворих [68].
Магнітно-резонансна томографія виявила в низки пацієнтів високий ступінь ураження білої речовини головного мозку, проте питання, чи це ураження спричинює власне SARS-CoV-2, чи гіпоксія через пошкодження судин, достеменно не вивчене. Отримано підтвердження, що SARS-CoV-2 може також провокувати розвиток енцефалопатії, менінгіту, гострого дисемінованого енцефаломієліту, судомних нападів, нейром’язових розладів, таких як синдром Гієна — Барре, полінейропатія, парези, атаксія. Частими неврологічними симптомами, що супроводжують COVID-19, також є запаморочення, головний біль, порушення свідомості [65].
Велике значення має розвиток ендотеліїту при COVID-19 — запального пошкодження судин, що спричинене вірусним ураженням ендотелію, гіперімунною реакцією (пошкодженням ендотелію цитокінами й вільними радикалами). Ендотеліїт, що супроводжується «тліючим» запаленням, — одна з основних причин тривалих постковідних ускладнень [69, 70]. Відомо, що дисфункція ендотелію відіграє істотну роль у процесах окисного стресу й апоптозу. Результатом окисного стресу і дисфункції ендотелію стає комплекс циркуляторних, метаболічних і нейротрофічних порушень [69, 70].
На сьогодні розроблено рекомендації щодо реабілітації пацієнтів у постковідному періоді, але в основному вони стосуються фізичної реабілітації, порад щодо зміни способу життя, харчування. Проводяться клінічні дослідження щодо вивчення ефективності лікарських препаратів у лікуванні неврологічних порушень у постковідних пацієнтів [21, 22, 71, 72]. Триває пошук нових лікарських засобів, які впливають на функцію ендотелію і мають протизапальну дію. До таких препаратів можна віднести Ксаврон® (едаравон) [73].
Експериментальні й клінічні дані свідчать про те, що Ксаврон® зменшує системне фонове запалення, пригнічує вивільнення прозапальних цитокінів, нейтралізує агресивні вільні радикали, зменшує активацію мікроглії, астроцитів, захищає ендотелій від пошкодження, активує eNOS, пригнічує функцію iNOS, nNOS; посилює адгезивні контакти ендотелію [74].
Отже, Ксаврон® може зменшувати «тліюче» системне запалення, ураження церебрального ендотелію, накопичення прозапальних цитокінів — фонове запалення, нейротропність самого вірусу SARS-CoV-2. А відомо, що ураження ендотелію провокує порушення коагуляційного гомеостазу, тромбоемболії, порушення метаболізму міокарда, розвиток інфарктів, міокардитів, інсультів [23, 75–77].
Є дані відносно того, що едаравон, якщо його своєчасно застосувати, зменшує ураження органів, клінічні ускладнення й смертність у випадках тяжкого перебігу COVID-19.
Незважаючи на багаторічний досвід застосування едаравону в неврології в лікуванні бокового аміотрофічного склерозу, ішемічного інсульту й накопичену за цей час доказову базу, що підтверджує його ефективність, інтерес дослідників до вивчення цього препарату не знижується. З огляду на патогенез постковідних порушень новим етапом наукових досліджень може стати вивчення ефективності едаравону у хворих, які перенесли COVID-19.
Додатковий ефект у лікуванні таких хворих може надати й Тіворель®. Препарат сприяє відновленню роботи серцево-судинної системи в постковідному періоді за рахунок L-аргініну та L-карнітину, які входять до його складу. L-аргінін відновлює ендотелій, зменшує спазм судин, запобігає тромбозу. L-карнітин покращує провідність і метаболізм міокарда. Завдяки синергії L-аргініну й L-карнітину покращується функція міокарда, підвищується толерантність до фізичних навантажень [78].
Для зменшення проявів астенії, що присутня в більшості пацієнтів у постковідному періоді, доцільним може бути додавання до вищенаведених лікарських засобів Ксилату. Ксилат® — незалежне від інсуліну джерело енергії. Ксилітол не впливає на рівень глюкози в крові, сприяє секреції ендогенного інсуліну. З 1 г ксилітолу продукується 837 кДж енергії. Він сприяє нормалізації водно-електролітного балансу.
Становить інтерес визначення ефективності комплексного застосування цих лікарських засобів у лікуванні постковідних пацієнтів.
Було проведено відкрите порівняльне дослідження ефективності комплексного застосування Ксаврону, Тіворелю й Ксилату в 30 пацієнтів з неврологічними порушеннями в постковідному періоді. Тривалість терапії становила 14 днів. Ксаврон® призначали по 30 мг 1 р/д на 100 мл NaCl 0,9% в/в. Тіворель® використовували в дозі 100 мл 1 р/д в/в, Ксилат® — 5–6 мл/кг 1 р/д в/в. Групу порівняння становили 30 пацієнтів з неврологічними порушеннями в постковідному періоді, які отримували стандартне базове лікування (вітамінотерапія, антигіпертензивна, гіпоглікемічна терапія, статини за показаннями, вазоактивні препарати).
Усі пацієнти завершили дослідження за відсутності побічних дій і змін з боку лабораторних показників.
Поряд з медикаментозною терапією пацієнтам були надані рекомендації щодо режиму роботи й відпочинку, дотримання режиму сну, правильного харчування, обмеження використання стимуляторів.
Дослідження проводилось у відділенні судинної патології головного мозку та реабілітації ДУ «Інститут неврології, психіатрії та наркології Національної академії медичних наук України». Воно було виконано відповідно до Гельсінської декларації, прийнятої в червні 1964 року й переглянутої в жовтні 2000 р. (Единбург, Шотландія). Усі пацієнти дали добровільну письмову інформовану згоду на участь у дослідженні.
Для визначення ефективності лікування пацієнтам основної групи й групи порівняння проводились наступні дослідження перед початком і після лікування:
- оцінка основних суб’єктивних клінічних проявів;
- дослідження неврологічного статусу;
- оцінка впливу лікування на психоемоційний стан пацієнтів;
- оцінка впливу лікування на когнітивні функції і якість життя;
- оцінка впливу лікування на рівень інтерлейкіну-6 і показник фактора росту ендотелію судин (VEGF).
Оцінка основних суб’єктивних клінічних проявів (головний біль, запаморочення, шум у голові, порушення сну, стомлюваність, забудькуватість, зниження настрою і тривожність, емоційна лабільність) проводилась з використанням 5-бальної рейтингової шкали зі стандартизованими критеріями оцінки вираженості кожного симптому: 0 балів — симптом відсутній, 1 бал — легкі прояви, 2 бали — помірно виражені, 3 бали — значно виражені, 4 бали — різко виражені.
Дослідження неврологічного статусу включало оцінку рухових, вестибуломозочкових, екстрапірамідних, чутливих і псевдобульбарних, вегетативних порушень за 5-бальною рейтинговою шкалою зі стандартизованими критеріями оцінки вираженості кожного симптому: 0 балів — симптом відсутній, 1 бал — легкі прояви, 2 бали — помірно виражені, 3 бали — значно виражені, 4 бали — різко виражені.
Прояви астенії оцінювали за допомогою опитувальника на втомлюваність — MFI-20, який дозволяє кількісно оцінити суб’єктивні відчуття астенії, а також ступінь загальної втоми, фізичної і розумової втомлюваності, редукції, мотивації та активності [79].
Психоемоційний стан оцінювали за допомогою шкали Спілбергера — Ханіна і шкали Гамільтона (HADS) [80].
Для дослідження когнітивних функцій використовували Монреальську шкалу когнітивних функцій (МоСА) [81].
Якість життя оцінювали за допомогою опитувальників SF-36 та EQ-5D [82].
З метою проведення диференціальної діагностики всім пацієнтам до початку лікування виконувалися комп’ютерна томографія або магнітно-резонансна томографія головного мозку, дуплексне сканування судин.
Концентрації інтерлейкіну-6 і фактора росту ендотелію судин визначали імуноферментним методом за допомогою відповідних наборів реагентів «Интерлейкин-6-ИФА-БЕСТ» і «VEGF-ИФА-БЕСТ» («Вектор-Бест», РФ) і виражали в пікограмах на мілілітр (пг/мл). Забір крові для отримання сироватки здійснювали перед початком лікування і через 14 днів лікування. Аліквоти сироватки крові заморожували при –80 °С і зберігали до вимірювання.
Отримані результати обробляли статистично, середні значення й стандартні відхилення обчислювали.
Статистичний аналіз відмінностей проводили з використанням t-тесту Стьюдента за умови з’ясування нормальності розподілу даних у вибірці. Значення р < 0,05 вважали значимим.
Результати дослідження
Пацієнти основної групи та групи порівняння до початку лікування були зіставлені за основними клінічними ознаками (табл. 1).
Хворі перенесли COVID-19 за 3–4 місяці до початку дослідження. Тяжкий перебіг захворювання був у 5 пацієнтів основної групи і 4 осіб групи порівняння. В основної кількості хворих перебіг гострого періоду COVID-19 був середнього й легкого ступеня тяжкості. Майже третина пацієнтів до зараження скаржились на головний біль, головокружіння, нестабільність артеріального тиску. Але після перенесеного COVID-19 ці скарги посилились і з’явились нові симптоми.
Таблиця 1. Порівняльна характеристика обстежених хворих до початку лікування
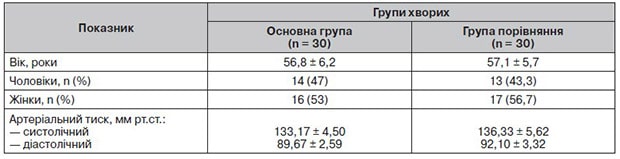
Таблиця 2. Динаміка суб’єктивних симптомів під час лікування
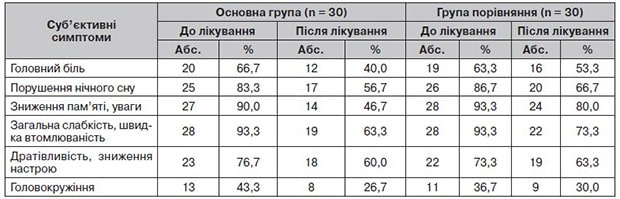
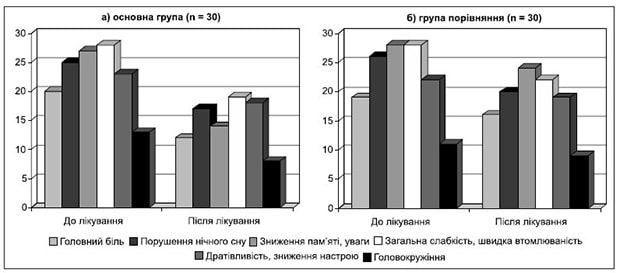
Рисунок 1. Динаміка суб’єктивних симптомів в основній (а) та контрольній (б) групах під час лікування
Найбільш частими скаргами в обстежених пацієнтів були: загальна слабкість, швидка й значна втомлюваність, зниження уваги, пам’яті, задишка, порушення нічного сну, головний біль, головокружіння, тривога, емоційна нестабільність. Скарги з’явились протягом 2–8 тижнів після гострого періоду захворювання.
Динаміка суб’єктивних порушень подана в табл. 2 та на рис. 1.
Позитивна клінічна ефективність лікування була відмічена в обох групах хворих, але в основній групі вона була значно більше виражена. Пацієнти відмітили, що в них зменшились втомлюваність, головний біль, головокружіння, тривога, значно покращився нічний сон.
Становило інтерес визначити не тільки частоту зустрічальності скарг хворих, але й оцінити ступінь їх вираженості після проведеного лікування. Після завершення лікування в більшості пацієнтів основної групи ступінь вираженості скарг знизився від 4 до 1–2 балів, у частини пацієнтів відмічалась повна редукція суб’єктивних проявів захворювання.
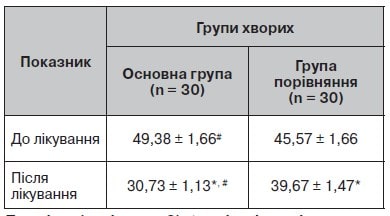
Таблиця 3. Оцінка вираженості астенії (MFI-20) до і після лікування
Примітки (тут і в рис. 2):
* — вірогідна різниця (p < 0,05) з показниками до початку лікування;
# — вірогідна різниця (p < 0,05) з показниками групи порівняння.
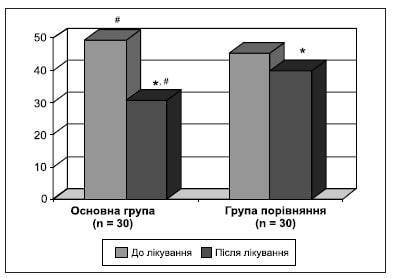
Рисунок 2. Динаміка вираженості астенії до та після лікування
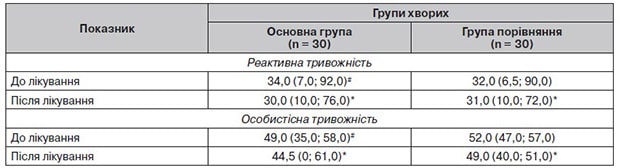
Таблиця 4. Динаміка показників загального бала за шкалою Спілбергера — Ханіна до і після лікування
Примітки (тут і в рис. 3):
* — вірогідна різниця (p < 0,05) з показниками до початку лікування;
# — вірогідна різниця (p < 0,05) з показниками групи порівняння.
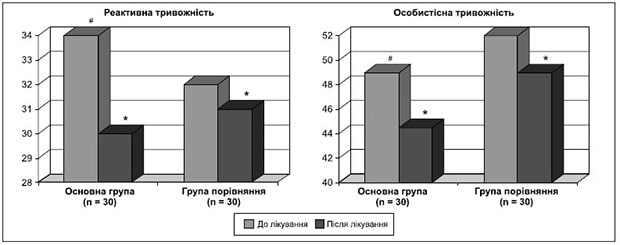
Рисунок 3. Динаміка показників загального бала за шкалою Спілбергера — Ханіна до і після лікування
При неврологічному огляді у хворих як основної групи, так і групи порівняння спостерігалась розсіяна мікровогнищева симптоматика. Можна було виділити основні синдроми — цефалгічний, астенічний, вегетосудинної дистонії, тривожний, когнітивних порушень. На момент включення в більшості пацієнтів мала місце виражена вегетативна лабільність, переважали збуджуючі вегетативні реакції.
Слід відмітити, що після лікування в основній групі частота зустрічальності й ступінь вираженості основних синдромів зменшились в цілому на 40 %, у групі порівняння — на 20 %. Найбільший вплив лікування в основній групі спостерігався щодо астенічного, цефалгічного синдромів, когнітивної дисфункції. Відмічалось зменшення вегетативних порушень, покращання координації.
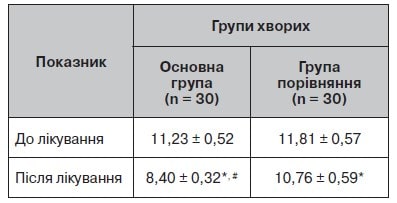
Таблиця 5. Динаміка депресивного синдрому за шкалою Гамільтона до і після лікування
Примітки (тут і в рис. 4):
* — вірогідна різниця (p < 0,05) з показниками до початку лікування;
# — вірогідна різниця (p < 0,05) з показниками групи порівняння.
Таблиця 6. Динаміка когнітивних функцій за шкалою МоСА до і після лікування (загальний бал)
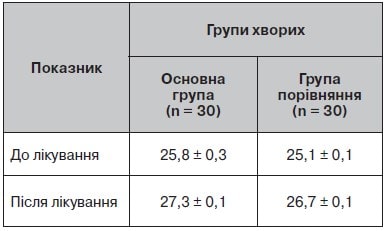
Рисунок 4. Динаміка депресивного синдрому за шкалою Гамільтона до і після лікування
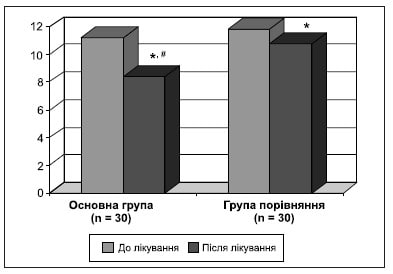
Рисунок 5. Динаміка когнітивних функцій за шкалою МоСА до і після лікування (загальний бал)
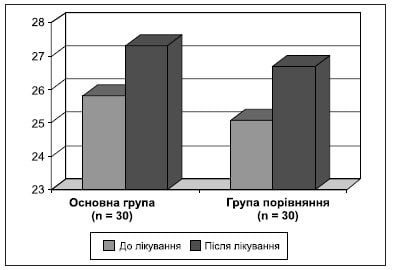
Таблиця 7. Оцінка якості життя EQ-5D до і після лікування
Примітки (тут і в рис. 6):
* — вірогідна різниця (p < 0,05) з показниками до початку лікування;
# — вірогідна різниця (p < 0,05) з показниками групи порівняння.
Рисунок 6. Оцінка якості життя EQ-5D до і після лікування
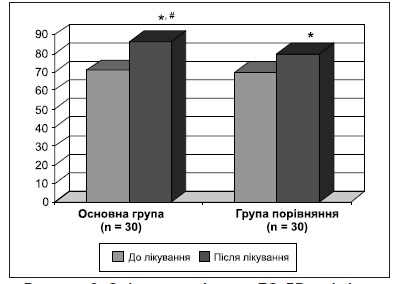
Найбільш частим серед неврологічних синдромів в обстежених хворих була астенія. Для оцінки її вираженості використовували шкалу MFI-20 (табл. 3).
Проведене лікування зменшило прояви вираженості астенії, значно більше у хворих основної групи.
У більшості пацієнтів були ознаки тривожного розладу. За допомогою шкали Спілбергера — Ханіна визначали рівень реактивної та особистісної тривожності. До лікування у хворих обох груп було виявлено помірний рівень реактивної і високий рівень особистісної тривожності.
Як видно з табл. 4, рис. 3, в обох групах спостерігалось зменшення рівня тривожності, але більш значно — в основній групі. У процесі лікування в обстежених хворих нормалізувався емоційний стан, зменшився рівень реактивної та особистісної тривожності.
Клінічні ознаки депресивного синдрому були в третини обстежених пацієнтів, про що свідчать показники за шкалою Гамільтона (табл. 5, рис. 4).
Після лікування вираженість депресивного синдрому зменшилась у всіх пацієнтів, але більше — в основній групі.
Більшість обстежених хворих скаржились на порушення пам’яті, уваги. Для їх об’єктивізації ми використовували Монреальську шкалу. Наші дослідження показали, що найбільше в обстежених пацієнтів постраждали увага й виконавчі функції. Особливо зміни стосувались уваги, швидкості обробки інформації, короткочасної робочої пам’яті. При цьому порушення уваги не були суттєво пов’язані з тяжкістю гострого періоду COVID-19, а більше залежали від віку пацієнтів.
Результат оцінки значень за шкалою MоСА в основній групі і групі порівняння до початку лікування свідчить про м’які й помірні порушення. В основній групі на тлі лікування виявлено статистично значуще покращання когнітивних функцій.
Таблиця 8. Динаміка показників якості життя за шкалою SF-36
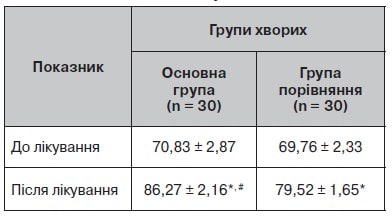
Рисунок 7. Динаміка показників якості життя за шкалою SF-36
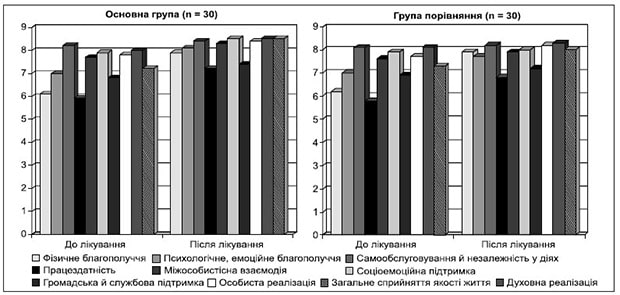
Таблиця 9. Динаміка С-реактивного білка до і після лікування (загальне значення), мг/л (норма від 0 до 6)
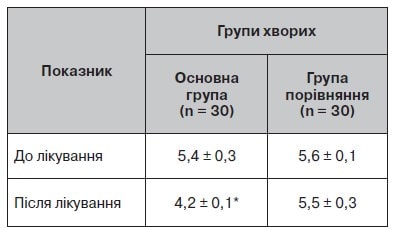
Примітка (тут і в рис. 8): * — різниця вірогідна (p < 0,05).
Рисунок 8. Динаміка С-реактивного білка до і після лікування (загальне значення), мг/л (норма від 0 до 6)
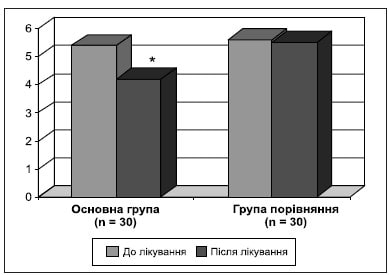
До кінця курсу лікування було встановлено статистично значуще покращання стану когнітивних функцій: збільшення темпу психічної діяльності, підвищення показників короткочасної та оперативної пам’яті (табл. 6, рис. 5).
Становила інтерес оцінка якості життя в обстежених хворих до і після лікування за допомогою шкал EQ-5D і SF-36 (табл. 7, 8, рис. 6, 7).
Для оцінки якості життя пацієнтів застосовувалася анкета-опитувальник SF-36 до і після лікування. Виявлено, що після лікування показники якості життя пацієнтів підвищуються в психічній і фізичній сферах (табл. 8, рис. 7). Динаміка показників якості життя під час лікування показала підвищення рівня психічного й фізичного здоров’я.
Дослідження С-реактивного білка сироватки крові показало, що в пацієнтів основної групи та групи порівняння цей показник був у межах норми (табл. 9, рис. 8). Після лікування він знизився в основній групі на 1,2 мг/л, що свідчило про протизапальний вплив комбінованої терапії.
При порівнянні концентрацій IL-6 у сироватці крові в абсолютних одиницях (пг/мл) у досліджених групах до і після відповідної терапії (рис. 9) було відмічено, що зміни середніх значень IL-6 спостерігаються в пацієнтів основної групи, тобто можна припустити, що запропонована нами схема лікування впливає на процеси запалення. Необхідно зауважити, що вірогідні зміни середніх значень показника фактора росту ендотелію судин спостерігаються в пацієнтів основної групи після лікування (рис. 9).
Становило інтерес визначити характер змін IL-6 і VEGF у пацієнтів з різним ступенем тяжкості гострого періоду COVID-19 (рис. 10). Тяжкі хворі мали вірогідно більші значення IL-6 і VEGF перед лікуванням порівняно з пацієнтами середньої тяжкості.
При цьому у хворих основної групи, які перенесли COVID-19 у тяжкій формі, показники IL-6 і VEGF були вищими порівняно з пацієнтами, у яких перебіг гострого періоду був середньої тяжкості. Такі особливості, можливо, обумовлені більшою вираженістю протизапального ефекту Ксаврону, Ксилату і Тіворелю саме в пацієнтів з тяжким перебігом гострого періоду COVID-19 з огляду на більший вплив саме на прозапальний цитокін IL-6.
Рисунок 9. Показники рівня IL-6 і VEGF у пацієнтів основної групи та групи порівняння Примітка: * — р < 0,05 при порівнянні показників до і після лікування.

Рисунок 10. Вплив лікування на рівень IL-6 і VEGF залежно від тяжкості перебігу гострого періоду в пацієнтів основної групи
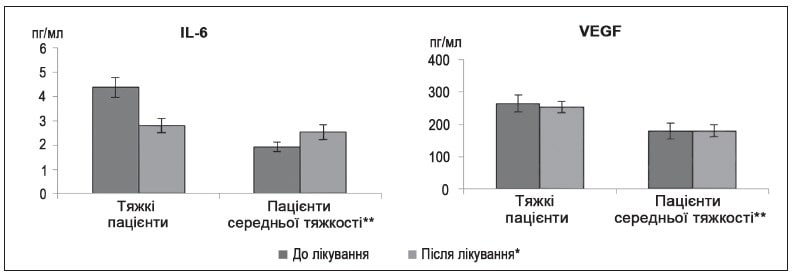
Примітки:
* — р < 0,05 при порівнянні показників до і після ексклюзивної терапії;
** — р < 0,05 при порівнянні показників тяжких пацієнтів і середньої тяжкості.
Отже, проведене нами дослідження показало, що наслідки перенесеного COVID-19 у вигляді астенічного, цефалгічного синдромів, когнітивних, психоемоційних порушень ще довго зберігаються в пацієнтів після гострого періоду захворювання. Такі порушення необхідно якомога швидше виявляти й корегувати. Включення до лікування таких пацієнтів препаратів Ксаврон®, Тіворель®, Ксилат® дозволяє зменшити прояви захворювання.
Клінічна ефективність підтверджується даними імуноферментного аналізу, що свідчать про позитивний вплив запропонованого комплексу на процеси запалення й ендотеліальну дисфункцію.
Висновки
- Комплексне застосування препаратів (Ксаврон®, Тіворель®, Ксилат®) чинило позитивний терапевтичний вплив на основні клінічні прояви в пацієнтів з постковідним синдромом.
- Запропонований комплекс лікування впливав на когнітивні функції, що виражалось у збільшенні темпу психічної діяльності, покращанні короткочасної і оперативної пам’яті, підвищенні стійкості психічних процесів. Лікування за такою схемою призводить до зниження рівня реактивної та особистісної тривожності.
- Показники якості життя пацієнтів при лікуванні такими препаратами збільшуються за рахунок фізичного й психічного компонентів.
- У постковідних пацієнтів з неврологічними ускладненнями сироваткові рівні прозапальних маркерних цитокінів IL-6 і VEGF були підвищеними. Додавання до базової терапії Ксаврону, Ксилату і Тіворелю обумовило зниження рівнів IL-6 і VEGF, що дає можливість висловити припущення про протизапальний вплив запропонованої нами схеми лікування.
- Ефективність і безпека препаратів Ксаврон®, Тіворель®, Ксилат® визначає перспективу їх призначення для лікування пацієнтів з неврологічними постковідними порушеннями.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів і власної фінансової зацікавленості при підготовці даної статті.
Список літератури
- Niu , Shen L., Huang B. et al. Non-invasive bioluminescence imaging of HCoV-OC43 infection and therapy in the central nervous system of live mice. Antiviral. Res. 2020. 173. 104646.
- Lodigiani , Iapichino G., Carenzo L. et al. Venous and arterial thromboembolic complications in COVID-19 patients admitted to an academic hospital in Milan, Italy. Thromb. Res. 2020. 191. 9-14.
- Hoffmann , Kleine-Weber H., Schroeder S., Krüger N., Herrler T., Erichsen S., Schiergens T.S., Herrler G., Wu N.H., Nitsche A., Müller M.A., Drosten C., Pöhlmann S. SARS-CoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a clinically proven protease inhibitor. Cell. 2020. 181(2). 271-280.e8.
- https://doi.org/10.1016/j.cell.2020.02.052.
- Rothan A., Byrareddy S.N. The epidemiology and pathogenesis of coronavirus disease (COVID-19) outbreak. J. Autoimmun. 2020. 109. 102433.
- Filatov , Sharma P., Hindi F. et al. Neurological complications of coronavirus disease (COVID-19): Encephalopathy. Cureus. 2020. 12(3). e7352.
- Ye , Ren Y., Lv T. Encephalitis as a clinical manifestation of COVID-19. Brain Behav. Immun. 2020. S0889-1591(20)30465-7.
- Moriguchi , Harii N., Goto J. et al. A first case of meningitis/ encephalitis associated with SARS-Coronavirus-2. Int. J. Infect. Dis. 2020. 94. 55-58.
- Duong , Xu P., Liu A. Meningoencephalitis without respiratory failure in a young female patient with COVID-19 infection in Downtown Los Angeles, early April 2020. Brain Behav. Immun. 2020. 87. 33.
- Zhao , Huang J., Dai D. et al. Acute myelitis after SARS-CoV-2 infection: a case report. MedRxiv. 2020.
- Wu , Xu X., Chen Z., Duan J., Hashimoto K., Yang L., Liu C., Yang C. Nervous system involvement after infection with COVID-19 and other coronaviruses. Brain Behav. Immun. 2020. 87. 18-22. doi: 10.1016/j.bbi.2020.03.031.
- Padroni , Mastrangelo V., Asioli G.M. et al. Guillain-Barré syndrome following COVID-19: new infection, old complication? [published online ahead of print, 2020 Apr 24]. J. Neurol. 2020. 1-3.
- Virani , Rabold E., Hanson T. et al. Guillain-Barré syndrome associated with SARS-CoV-2 infection [published online ahead of print, 2020 Apr 18]. IDCases. 2020. 20. e00771.
- Camdessanche P., Morel J., Pozzetto B. et al. COVID-19 may induce Guillain-Barré syndrome. Rev. Neurol. (Paris). 2020. 176(6). 516-518.
- Sedaghat , Karimi N. Guillain Barre syndrome associated with COVID-19 infection: A case report. J. Clin Neurosci. 2020. 76. 233-235.
- Nguyen-Huynh N., Tang X.N., Vinson D.R. et al. Acute Stroke Presentation, Care, and Outcomes in Community Hospitals in Northern California During the COVID-19 Pandemic. Stroke (IF 7.190). Pub Date: 2020-08-07. DOI: 10.1161/ strokeaha.120.031099.
- Li Y. Acute cerebrovascular disease following COVID-19: a single center, retrospective, observational study. SSRN J. 2020.
- Mao , Jin H., Wang M., Hu Y., Chen S., He Q., Chang J., Hong C., Zhou Y., Wang D., Miao X., Li Y., Hu B. Neurologic manifestations of hospitalized patients with coronavirus disease 2019 in Wu- han, China. JAMA Neurol. 2020. e201127. https://doi.org/10.1001/ jamaneurol.2020.1127.
- Міщенко Т.С., Міщенко В.М. Неврологічні ускладнення у пацієнтів з COVID-19. Міжнародний науково-практичний журнал «Психіатрія, неврологія та медична психологія» ХНУ ім. В.Н. Каразіна. № 16. С. 23-33.
- Espinosa P.S., Rizvi , Sharma P., Hindi F., Filatov A. Neurological Complications of Coronavirus Disease (COVID-19): Encephalopathy, MRI Brain and Cerebrospinal Fluid Findings: Case 2. Cureus. 2020. 12. e7930.
- Tay Z., Poh C.M., Rénia L., MacAry P.A., Ng L.F.P. The trinity of COVID-19: immunity, inflammation and intervention. Nat. Rev. Immunol. 2020. 20. 363-74. doi:10.1038/s41577-020-0311-8 pmid: 32346093. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7187672/
- Barker-DaviesM., O’Sullivan O., Senaratne K.P. et al. The Stanford Hall consensus statement for post-COVID-19 rehabilitation. Br. J. Sports Med. 2020. 54. 949-959.
- Gemelli Against COVID-19 Post-Acute Care Study Post-COVID-19 global health strategies: the need for an interdisciplinary approach. Aging Clinical and Experimental Research. https:// doi.org/10.1007/s40520-020-01616-x.
- Reznik E. et al. Edaravone: A potential treatment for the COVID-19-induced induced inflammatory syndrome? Pharmacol. Res. 2020 Jun 30. 160. 105055.
- Johns Hopkins Coronavirus Resource Center. Accessed at https://coronavirus.jhu.edu/map.html.
- Chu , Chan J.F., Yuen T.T. et al. Comparative tropism, replication kinetics, and cell damage profiling of SARS-CoV-2 and SARS-CoV with implications for clinical manifestations, transmissibility, and laboratory studies of COVID-19: an observational study. Lancet Microbe. 2020. 1(1). 14-23.
- Hashimoto , Sanui M., Egi M. et al. The clinical practice guideline for the management of ARDS in Japan. J. Intensive Care. 2017. 5. 50.
- Saito , Fujii Y., Yashiro M. et al. Inhibitory Effects of Edaravone, a Free Radical Scavenger, on Cytokineinduced Hyperpermeability of Human Pulmonary Microvascular Endothelial Cells: A Comparison with Dexamethasone and Nitric Oxide Synthase Inhibitor. Acta Med. Okayama. 2015. 69(5). 279-290.
- Kanjanaumporn, Aeumjaturapat S., Snidvongs K., Seresirikachorn K., Chusakul S. Smell and taste dysfunction in patients with SARSCoV-2 infection: A review of epidemiology, pathogenesis, prognosis, and treatment options. Asian Pac. J. Allergy Immunol. 2020. 38. 69-77.
- Cantuti-Castelvetri , Ojha R. et al. Neuropilin-1 facilitates SARS-CoV-2 cell entry and infectivity. Science. 2020. 370. 856-860.
- Adamczyk-Sowa , Niedziela N., Kubicka-Baczyk K., Wier- zbicki K., Jaroszewicz J., Sowa P. Neurological symptoms as a clinical manifestation of COVID-19: Implications for internists. Polish Arch. Intern. Med. 2020.
- Alquisiras-Burgos , Peralta-Arrieta I., Alonso-Palomares L.A. et al. Neurological Complications Associated with the Blood-Brain Barrier Damage Induced by the Inflammatory Response During SARS-CoV-2 Infection. Mol. Neurobiol. 2021. 58. 520-535. https://doi.org/10.1007/s12035-020-02134-7.
- Al-Sarraj S., Troakes C., Hanley B., Osborn M., Richard- son P., Hotopf M., Bullmore E., Everall I.P. Invited Review: The spectrum of neuropathology in COVID-19. Neuropathol. Appl. Neurobiol. 2021 Feb. 47(1). 3-16. doi: 10.1111/nan.12667. Epub 2020 Oct PMID: 32935873.
- Poyiadji , Shahin G., Noujaim D., Stone M., Patel S., Griffith B. COVID-19-associated acute hemorrhagic necrotizing encephalopathy: CT and MRI features. Radiology. 2020. 201187.
- Дзяк Л.А., Цукаленко О.С., Чеха К.В., Сук В.М. Сучасні аспекти нейрогенезу й неврологічних проявів COVID-19. Міжнародний неврологічний журнал. 2021. Т. 17. № 2. С. 6. DOI:https://org/10.22141/22240713.17.2.2021.229887.
- Зозуля І.С., Мардзвік В.М., Мардзвік М.В. Судинні неврологічні ускладнення в пацієнтів з COVID-19. Український медичний часопис. ІІ/IV. 2(142). DOI: 10.32471/umj.1680- 3051.142.204731.
- Копчак О.О. Особливості когнітивних порушень при COVID-19. Міжнародний неврологічний журнал. 2021. Т.№3.С.12.DOI:http://dx.doi.org/https://doi.org/10.22141/2224-0713.17.3.2021.231569.
- Oliveira et al. Neuro-COVID frequency and short-term outcome in the northern Portuguese population. European Journal of Neurology. https://doi.org/10.1111/ene.14874.
- Fartushna Yе., Palahuta H.V., Yevtushenko S.K. Neurological and neuropsychiatric manifestations and complications of SARS-CoV-2 infection: a narrative review and a case presentation in a previously healthy young white adult. Міжнародний неврологічний журнал. 2021. Т. 17. № 1. С. 36. DOI: https://doi. org/10.22141/2224-0713.17.1.2021.226914.
- Panariello , Cellini L., Speciani M., De Ronchi D., Atti A.R. How Does SARS-CoV-2 Affect the Central Nervous System? A Working Hypothesis. Front Psychiatry. 2020. 11. 582345. Published 2020 Nov 16. doi: 10.3389/fpsyt.2020.582345.
- Zhou , Zhang M., Wang J. et al. Sars-CoV-2: Underestimated damage to nervous system [published online ahead of print, 2020 Mar 24]. Travel Med. Infect. Dis. 2020. 101642.
- Pilotto , Odolini S., Masciocchi S. et al. Steroidresponsive encephalitis in coronavirus disease 2019 [published online ahead of print, 2020 May 17]. Ann. Neurol. 2020. 10.1002/ana.25783.
- Lin Y., Lee K.Y., Ro L.S., Lo Y.S., Huang C.C.,Chang K.H. Clinical and cytokine profile of adult acute necrotizing encephalopathy. Biomed J. 2019. 42(3). 178-186. https://doi. org/10.1016/j.bj.2019.01.008.
- Klok A., Kruip M., van der Meer N.J.M., Arbous M.S., Gommers D., Kant K.M. et al. Incidence of thrombotic complications in critically ill ICU patients with COVID-19. Thromb. Res. 2020. 191. 145-7.
- Asadi-Pooya A., Simani L. Central nervous system manifestations of COVID-19. A systematic review. J. Neurol. Sci. 2020. 413. 116832.
- Carfì , Bernabei R., Landi F., Group ftGAC-P-ACS. Persistent Symptoms in Patients After Acute COVID-19. J. Am. Med. Assoc. 2020. 324(6). 603-605. DOI: 10.1001/jama.2020.12603.
- Armocida , Pesce A., Raponi I., Pugliese F., Valentini V., Santoro A., Berra L.V. Anosmia in COVID-19: severe acute respiratory syndrome coronavirus 2 through the nasoliary epithelium and a possible spreading way to the central nervous system — A purpose to study. Neurosurgery. 2020. https://doi.org/10.1093/neuros/nyaa204.
- Mahalaxmi , Kaavya J., Mohana Devi S., Balachandar V. COVID-19 and olfactory dysfunction: A possible associative approach towards neurodegenerative diseases. J. Cell. Physiol. 2021. 236. 763-770. https://doi.org/10.1002/jcp.29937.
- Parry H., Wani A.H., Yaseen M. Neurological Dysfunction in Coronavirus Disease-19 (COVID-19). Acad. Radiol. 2020. 27. 1329-1330.
- Huang , Wang Y., Li X. et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020. 395. 497-506.
- Helms , Kremer S., Merdji H. et al. Neurologic features in severe SARS-CoV-2 infection. N. Engl. J. Med. 2020. 382(23). 2268- 2270.
- Тріщинська М.А., Кононов О.Є., Бельська І.В. Патогенетично обгрунтована профілактика цереброваскулярних захворювань у хворих із коронавірусною інфекцією. Міжнародний неврологічний журнал. Т. 16. № 7. С. 23-31.
- Лунева И.Е., Полищук Р.В., Чернобаева Л.С., Бормин А.А., Антипят Н.А., Рябинкина Ю.В., Пирадов М.А. Острый некротический энцефалит, ассоциированный с вирусом гриппа, у взрослых. Журнал неврологии и психиатрии им. С.С. Корсакова. 2020. 120(4). 101-105. https://doi.org/10.17116/jnevro2019119121100.
- Wang L., Iwanami J., Min L.J., Tsukuda K., Nakaoka H., Bai H.Y., Shan B.S., Kan-No H., Kukida M., Chisaka T., Ya- mauchi T., Higaki A., Mogi M., Horiuchi M. Deficiency of angio- tensin-converting enzyme 2 causes deterioration of cognitive func- tion. NPJ Aging Mech. Dis. 2016. 2. 16024. https://doi.org/10.1038/ npjamd.2016.24.
- Ayoubkhani , Khunti K., Nafilyan V., Maddox T., Humberstone B., Diamond I. et al. Post-COVID syndrome in individuals admitted to hospital with COVID-19: retrospective cohort study. BMJ. 2021. 372. n693. doi: 10.1136/bmj.n693
- Greenhalgh , Knight M., A’Court C., Buxton M., Husain L. Management of post-acute covid-19 in primary care. Br. Med. J. 2020. 370. m3026. DOI: 10.1136/bmj.m3026.
- СOVID-19 rapid guideline: managing the long-term effects of COVID-19. NICE guideline [NG188]. Published date: 18 December 2020. https://www.nice.org.uk/guidance/ng188/chapter/5-Management.
- Lopez-Leon , Wegman-Ostrosky T., Perelman С., Sepulveda R., Rebolledo P.A., Cuapio А., Villapol S. More than 50 Longterm effects of COVID-19: a systematic review and meta-analysis. Doi: https://doi.org/10.1101/2021.01.27.21250617.
- Sharma , Lioutas V.-A., Madsen T., Clark J., O’Sullivan J., Elkind M.S.V., Willey J.Z., Marshall R.S., Selim M.H., Greer D., Tirschwell D.L., Burton T., Boehme A. Decline in stroke alerts and hospitalisations during the COVID-19 pandemic. Stroke Vasc Neurol. 2020 Dec. 5(4). 403-405. Article in English | MEDLINE | ID: covidwho-1318203.
- Guedj , Campion J.Y., Dudouet P. 18F-FDG brain PET hypometabolism in patients with long COVID. Eur. J. Nucl. Med. Mol. Imaging. 2021. https://doi.org/10.1007/s00259-021-05215-4.
- Carvalho-Schneider , Laurent E., Lemaignen A., Beaufils E., Bourbao-Tournois C., Laribi S. et al. Follow-up of adults with noncritical COVID-19 two months after symptom onset. Clin. Microbiol. Infect. 2020. DOI: 10.1016/j.cmi.2020.09.052.
- Spinato , Fabbris C., Polesel J. et al. Alterations in Smell or Taste in Mildly Symptomatic Outpatients with SARS-CoV-2 Infection. JAMA. 2020. 323(20). 2089-2090.
- Noor-Ul-Huda , Ain S., Salman Y. The Effects of COVID-19 on Hypothalamus: Is it Another Face of SARS-CoV-2 That May Potentially Control the Level of COVID-19 Severity? DOI: 10.13140/RG.2.2.24482.25289.
- Goërtz M.J., Van Herck M., Delbressine J.M., Vaes A.W., Meys R., Machado F.V.C. et al. Persistent symptoms 3 months after a SARS-CoV-2 infection: the post-COVID-19 syndrome? ERJ Open Res. 2020. DOI: 10.1183/23120541.00542-2020.
- Голубовська О.А. Постковідний синдром: патогенез та основні напрями реабілітації. Здоров’я України 21 сторіччя.№ 3(496).
- Paterson W., Brown R.L., Manji H., Zandi M.S. Contrib- uted equally to this work. Brain. 2020. Vol. 143. Issue 10. https://doi. org/10.1093/brain/awaa240.
- Weir К. COVID-19 attacks the brain. Monitor on Psychology. Vol. 51. № 8. Р. 20.
- Branca М. Early details of brain damage in COVID-19 patients. The Harvard Gazette. November 18, 2020.
- Baird S., Montine T.J. Multiplex immunoassay analysis of cytokines in idiopathic inflammatory myopathy. Arch. Pathol. Lab. Med. 2008. 132(2). 232238.
- Varga , Flammer A.J., Steiger P. et al. Endothelial cell infection and endotheliitis in COVID-19. The Lancet. 2020. 395(2). 1417-1418.
- Desforges , Le Coupanec A., Stodola J.K. Human coronaviruses: viral and cellular factors involved in neuroinvasiveness and neuropathogenesis. Virus Res. 2014 Dec 19. 194. 145-58.
- Najjar , Najjar A., Chong D.J. et al. Central nervous system complications associated with SARS-CoV-2 infection: integrative concepts of pathophysiology and case reports. Journal of Neuroinflammation. 2020. 17. 231.
- Zhang , Zhao Y., Zhang F. The use of anti-inflammatory drugs in the treatment of people with severe coronavirus disease 2019 (COVID-19): The Perspectives of clinical immunologists from China. Clinical Immunology. 2020. 214. 108393.
- Yang Y. Edaravone Alleviated Propofol-Induced Neurotoxicity in Developing Hippocampus by mBDNF/TrkB/PI3K Pathway. Drug Devel. Ther. 2021. 15. 1409-1422.
- Негрич Т.І. Застосування препаратів едаравону, цитиколіну й електролітів та L-аргініну в пацієнтів із гострим порушенням мозкового кровообігу. НейроNEWS. 2020. 9(120). 12-19.
- Watanabe et al. How is edaravone effective against acute ischemic stroke and amyotrophic lateral sclerosis? J. Clin. Biochem. Nutr. 2018 Jan. 62(1). 20-38
- Znong H. Efficacy and safety of current therapeutic options for COVID-19lessons to be learnt from SARS and MERS epidemic: A systematic review and meta-analysis. Pharmacol Res. 2020 Jun. 157.
- Загайко А.Л., Брюханова Т.О., Шинкарьов А.А., Мельник Н.В. Метаболічні ефекти карнітину, роль у розвитку патологій та перспективи клінічного застосування (огляд). Український біофармацевтичний журнал. № 6.
- Smeis M., Garssen B.J., Bonke B., DeHaes J.C. Піе multidimensional fatigue inyentory (MFI) psychometric qualities of an instrument to assess fatigue. Journal of Psychosomatic Research. 1995. 39. 315-325.
- Ханин Ю.Л. Краткое руководство к применению шкалы реактивной личностной тревожности Ч.Д. Спилбергера. Л.: ЛНИИФК, 1976.
- Nasreddine S., Phillips N.A., Bédirian V., Charbonneau S., Whitehead V., Collin I., Cummings J.L., Chertkow H. The Montreal Cognitive Assessment, MoCA: a brief screening tool for mild cognitive impairment. J. Am. Geriatr. Soc. 2005. 53(4). 695-699. https://doi. org/10.1111/j.1532-5415.2005.53221.x.
- Brazier , Roberts J., Deverill M. The estimation of a preference-based measure of health from the SF-36. J. Health Econ. 2002. 21(2). 271-292. https://doi.org/10.1016/s0167-6296(01)00130-8.
Опубліковано: Міжнародний неврологічний журнал, Том 17, N 6, 2021